美國輔助生殖紡錘體卵質量評估
通過抑制細胞周期重新進入,可以減少神經元的細胞凋亡,保護神經元的存活。例如,使用細胞周期抑制劑(如CDK抑制劑)可以抑制細胞周期重新進入,減少神經元的細胞凋亡。此外,通過促進神經元的細胞周期退出,也可以減少神經元的細胞凋亡。通過改善線粒體功能,可以恢復能量代謝,保護神經元的存活。例如,使用線粒體功能增強劑(如輔酶Q10)可以改善線粒體功能,恢復能量代謝。此外,通過減少線粒體的氧化應激,也可以改善線粒體功能。紡錘體,作為細胞分裂的“引擎”,驅動著生命的延續與多樣性。美國輔助生殖紡錘體卵質量評估
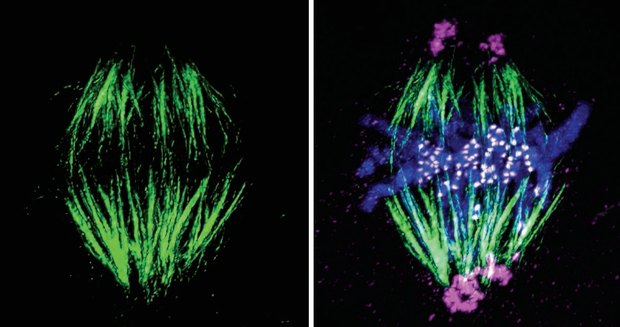
染色體非整倍性是指細胞中染色體數目異常,即染色體數目不是正常二倍體數目的整數倍。這種異常在多種疾病中都可見,包括遺傳性疾病和不孕不育等。紡錘體是細胞分裂過程中負責染色體分離的關鍵結構,其功能缺陷可能導致染色體非整倍性的發生。紡錘體是由微管、動力蛋白和調節蛋白等組成的動態結構,負責在有絲分裂和減數分裂過程中確保染色體的正確分離和分配。紡錘體的主要功能包括:染色體捕捉:紡錘體通過動粒微管(kinetochoremicrotubules)捕捉染色體的著絲粒,確保染色體在分裂中期排列在赤道板上。染色體分離:紡錘體通過極微管(polarmicrotubules)和動粒微管的動態變化,推動染色體在分裂后期向兩極移動,實現染色體的均等分配。細胞分裂:紡錘體還參與細胞分裂的其他過程,如細胞質分裂(cytokinesis)。深圳卵母細胞紡錘體胚胎發育紡錘體在細胞分裂后期推動染色體向細胞兩極移動。
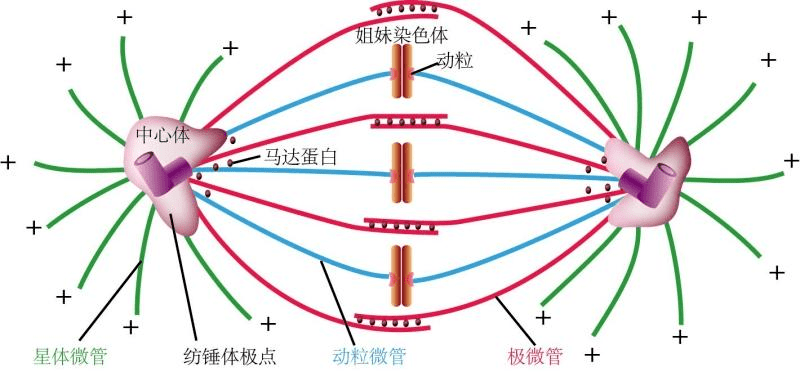
多極紡錘在有絲分裂時紡錘體一般有二個極。但是在多精入卵的卵細胞、腫瘤細胞、培養的HeLa細胞、雜種細胞等,隨著條件不同可形成有3、4個或者更多個極的紡錘體。當存在多極紡錘體時,染色體的后期分配便不規則,可形成幾個小核。用低濃度的秋水仙堿等藥物處理也能誘導出同樣的變化。木賊等特殊的植物體或胚乳細胞,往往在分裂初期形成多極紡錘體,及至分裂中期多數可恢復為二個極。長期以來,科學家認為在哺乳動物胚胎的***次細胞分裂過程中,只有一個紡錘體負責將胚胎染色體分配到兩個細胞中。但歐洲研究人員利用小鼠開展的**近實驗觀察發現,這個過程中實際上有兩個紡錘體,分別負責來自父親和母親的染色體[2]。雙紡錘體的形成可能部分解釋了為什么哺乳動物在早期發育階段(胚胎*初的幾次細胞分裂中)會有非常高的錯誤率。如果紡錘體的兩極沒有對齊和融合,那么,受精卵的遺傳物質可能會被拉向3個或4個方向,而不是2個。而這種錯誤會導致擁有多個細胞核的細胞產生,從而終止胚胎發育。雙紡錘體理論的提出提供了一種先前未知的機制。接下來需要探討的是雙紡錘體是否在人類中也發揮相同的作用。因為,這將為研究如何改善人類不育***提供非常有價值的信息[3]。
核移植,又稱體細胞核移植,是一種將體細胞的細胞核移入去核卵母細胞中的技術。這一技術的關鍵在于確保移植后的細胞核能夠在卵母細胞內重新編程,恢復全能性,并引導后續的胚胎發育。自1996年克隆羊“多莉”誕生以來,核移植技術便引起了全球范圍內的關注與研究熱潮。紡錘體是卵母細胞在減數分裂過程中形成的關鍵結構,負責精確分離染色體,確保遺傳信息的正確傳遞。然而,紡錘體對外部環境極為敏感,容易受到冷凍過程中溫度波動、滲透壓變化及冷凍保護劑毒性等因素的影響而發生損傷。因此,紡錘體卵冷凍技術的成功與否,直接關系到核移植后胚胎的發育潛力和質量。紡錘體在細胞分裂中的功能受到嚴格的時間和空間控制。
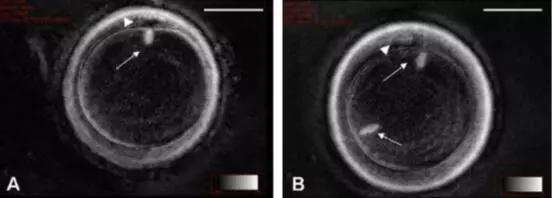
近年來,研究者們通過不斷優化冷凍保護劑的配方和濃度,發現某些特定成分的組合能夠減輕冷凍過程中紡錘體的損傷。例如,紫杉醇等細胞骨架保護劑在穩定紡錘體微管結構方面表現出色,成為冷凍保存中的重要輔助手段。Polscope偏振光顯微成像系統的應用,使得對雙折射性紡錘體的動態觀察成為可能。通過實時監測冷凍過程中紡錘體的形態變化,研究者能夠更準確地評估冷凍效果,并優化冷凍保存條件。此外,偏光成像技術還能夠提供紡錘體異常率的量化數據,為臨床應用提供可靠依據。紡錘體的形成需要多種蛋白質的參與,包括微管相關蛋白和中心體蛋白等。北京紡錘體實時成像紡錘體Oosight Meta
紡錘體微管網絡的形成和維持需要消耗大量能量。美國輔助生殖紡錘體卵質量評估
哺乳動物卵母細胞的紡錘體由微管組成,這些微管結構精細且高度動態,對溫度、滲透壓和機械力等外界因素極為敏感。在冷凍過程中,紡錘體容易因冰晶形成、滲透壓變化或機械損傷而遭到破壞,導致染色體分離異常,進而影響卵母細胞的發育潛力和受精后的胚胎質量。選擇合適的冷凍保護劑是減少紡錘體損傷的關鍵。然而,不同濃度的冷凍保護劑對紡錘體的影響各異,且不同哺乳動物種類之間也存在差異。因此,需要通過大量實驗來優化冷凍保護劑的配方,以大限度地保護紡錘體的完整性。美國輔助生殖紡錘體卵質量評估
- 馬精子分析WOB 2025-07-10
- 北京精子分析頻閃光源 2025-07-08
- 北京紡錘體實時成像紡錘體改善分級 2025-07-08
- 昆明無需染色紡錘體改善分級 2025-07-08
- 上海紡錘體胚胎植入 2025-07-08
- 深圳非侵入式成像紡錘體胚胎植入 2025-07-08
- 香港偏光成像紡錘體揭示卵母細胞關鍵結構 2025-07-08
- 北京核移植紡錘體 2025-07-08
- 美國哺乳動物紡錘體兼容大部分顯微鏡 2025-07-08
- 偏光成像紡錘體觀測儀 2025-07-08
- 生產自動化醫療器械材料分析系統 2025-07-12
- 河南OBD汽摩配件廠 2025-07-12
- 南通890-920nm多角度分光鏡類型 2025-07-12
- 耐酸堿襯氟對夾式蝶閥品牌 2025-07-12
- 西安智能化VOC在線監測報價 2025-07-12
- 廢舊鋰電池分析儀維修 2025-07-12
- 江西評估產品性能高溫試驗箱功率 2025-07-12
- 工業自動化螢石光譜分析儀 2025-07-12
- 黑龍江溫度儀表 2025-07-12
- 靜安區特制儀器儀表銷售調試 2025-07-12