徐匯區仿制藥eCTD服務介紹
電子簽章與傳輸安全 文件需經AES-256加密后刻錄至不可擦寫光盤,并附MD5校驗碼。光盤損壞或病毒污染將觸發重遞交流程,原載體按銷毀程序處理。 ?審評與核查協同 自2018年起,FDA要求提交兩套光盤分別用于審評和現場核查,2022年調整為“1套審評+1套核查+1套專項資料”模式,提升流程效率。 ?國際化兼容性增強 美國eCTD系統支持與歐盟、日本等地區的XML互操作性,但區域差異(如模塊1的標簽要求)仍需人工適配。 ?未來通道創 FDA計劃引入API接口支持企業系統直連,并探索基于云存儲的實時提交與審評,減少物理媒介依賴。澳大利亞eCTD申報軟件相關技術支持。徐匯區仿制藥eCTD服務介紹

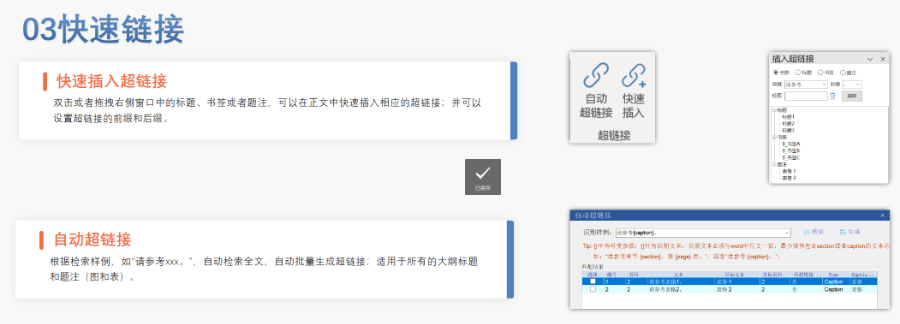
eCTD的技術架構與模塊要求:美國eCTD基于XML技術,嚴格遵循ICH M4框架,分為5個模塊:模塊1(地區行政信息)、模塊2(技術總結)、模塊3-5(質量、非臨床與臨床數據)。其中,模塊1需包含FDA特定的文件,涵蓋申請編號、聯系人和DMF授權書等行政信息。模塊2-5需與ICH CTD全球統一標準一致,但FDA對文件顆粒度要求更細,例如非臨床研究報告需拆分并標記Study ID。PDF文件需符合FDA v4.1格式規范,包括字體嵌入、書簽層級和超鏈接功能。蕪湖INDeCTD哪家好eCTD申報相關技術支持。
美國電子提交通道ESG(Electronic Submissions Gateway)是美國食品藥品監督管理局(FDA)建立的電子化監管信息提交系統,旨在為制藥、生物制品、醫療器械等行業提供安全、高效的電子申報服務。自2006年啟用以來,ESG已成為FDA接收電子監管材料的入口,每日處理上千份提交文件,涵蓋上市前審批、上市后監管、臨床試驗數據、不良反應報告等多種類型。該系統通過數字證書加密和公鑰基礎設施(PKI)技術,確保文件傳輸的真實性、完整性和不可否認性,符合FDA對電子提交的嚴格合規要求。在技術層面,ESG具備強大的文件處理能力。2018年系統升級后,取消了單個文件8GB的限制,可支持高達35GB的大型文件提交,進一步滿足復雜申報需求。此外,文件格式需遵循eCTD(電子通用技術文檔)規范,包括模塊化結構、PDF標準化和XML元數據整合,以確保全球監管機構兼容性。2025年3月28日起,FDA將啟用新一代平臺ESG NextGen,逐步替代現有系統,過渡期需關注兼容性和穩定性問題。
DMF維護與合規 ?年度更 即使無變更,每年需提交聲明;重大工藝/設施變更需及時通知客戶并更文件。 ?現場檢查 原料藥企業需通過FDA現場檢查,驗證是否符合ICH Q7 GMP標準,并與DMF內容一致。 ?轉讓與關閉 ?轉讓:需書面通知FDA并提供持有者信息。 ?關閉:未提交年度報告或持有人主動申請,需說明原因并通知所有授權方。 關鍵注意事項 ?數據質量:所有資料需準確、完整,減少審核延遲風險。 ?合規性:遵循FDA指南(如21 CFR Part 207)及USP標準(如培養基物料來源級別)。 ?溝通機制:建議通過專業機構(如瑞歐佰藥)協助,定期提交周報并制定計劃表以提高效率。 常見問題解答 ?生物制品分類:培養基、外泌體等均屬Ⅱ類DMF。 ?質量標準:參考USP及同行標準,需提供分析方法驗證及雜質對比研究。 ?周期估算:資料準備約5-50個工作日,總周期受缺陷回復影響。美國IND注冊申報相關技術支持。
eCTD生命周期管理與變更提交:歐盟要求eCTD申報資料覆蓋藥品全生命周期,包括提交、補充申請及實質性變更。例如,增成員國需提交“附加成員國序列”,審評時間約52-83天;重大變更(如生產工藝調整)需創建序列并通過CTIS平臺更模塊3和模塊1的GMP證明。技術驗證工具(如EDQM推薦的檢查軟件)需在每次提交前運行,確保XML骨架文件與PDF書簽層級符合規范。此外,電子簽章需符合《歐盟電子簽名法》,并在模塊1中明確標注法律效力。歐洲通用提交門戶(Common European Submission Portal,CESP)是歐盟及成員國藥品監管機構間用于電子化提交申報資料的重要平臺。以下是關于CESP的詳細介紹: CESP是由歐盟藥品監管部門負責人網絡(HMA)合作開發的在線交付系統,旨在為藥品注冊申請者、利益相關方和監管機構之間提供統一、安全的電子提交通道。其設計初衷是簡化跨國申報流程,允許通過單一門戶向多個歐洲國家的藥監部門同時提交申請,避免了重復操作。歐盟eCTD注冊咨詢相關技術支持。徐匯區INDeCTD系統
澳大利亞eCTD驗證標準相關技術支持。徐匯區仿制藥eCTD服務介紹
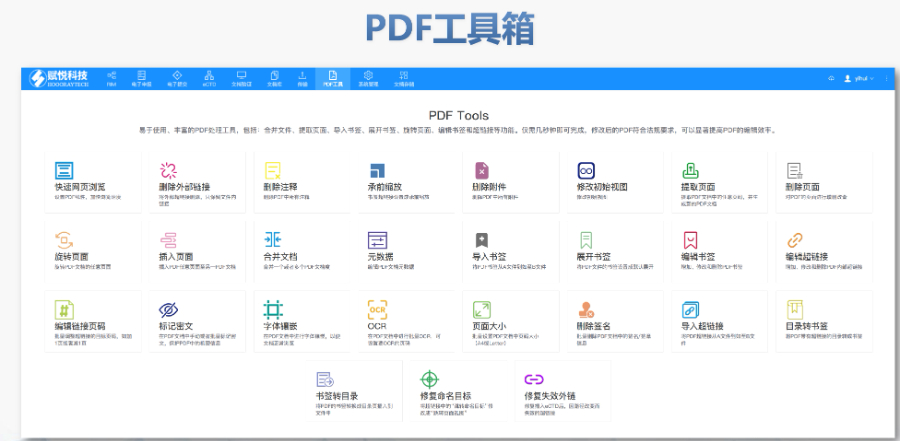
賦悅eCTD系統 ?文件驗證與修復 支持自動驗證文件格式(如PDF屬性、字體嵌入、超鏈接完整性等),并一鍵修復不符合法規要求的文件。例如,系統會自動檢查XML主干文件的結構合規性,確保符合中國、美國、歐盟等地區的eCTD法規標準。 ?eCTD組裝與發布 可自動生成符合CTD結構的電子文檔包,包括XML主干文件、文件夾命名規范及序列號管理(如申請號/序列號文件夾自動生成),并支持超鏈接和書簽的批量創建。例如,初次提交的序列號為0000,后續每次提交自動遞增。 ?生命周期管理 支持文件全生命周期操作(增、增補、替換、刪除),并通過序列號疊加直觀顯示各章節文件的有效性,覆蓋從初次提交到年報、撤市的全流程管理。 ?協同與權限管理 基于B/S架構(瀏覽器/服務器),支持云端或本地靈活部署,全集團賬號通用。提供多用戶協作功能,包括權限分級、審計追蹤、文件版本控制等。 ?法規支持與專業服務 內置符合中國CDE、美國FDA、歐盟EMA等法規的模板,同時提供注冊咨詢、資料撰寫、eCTD格式代轉等全流程支持,團隊擁有17年藥品注冊經驗。徐匯區仿制藥eCTD服務介紹
- 黑龍江化學藥品eCTD 2025-07-16
- 工業園區化學藥品eCTD名稱 2025-07-16
- 南京中國eCTD系統 2025-07-16
- 高新區中國eCTD歡迎選購 2025-05-14
- 靜安區生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區賦悅科技eCTD供應商 2025-05-14
- 南京生物制品eCTD注冊系統 2025-05-14
- 上海化學藥品eCTD格式 2025-05-09
- 南京電子申報eCTD哪個品牌好 2025-05-09
- 安徽物流軟件系統參數 2025-07-18
- 常熟進口電腦整機設置 2025-07-18
- 東莞vr虛擬制片軟件報價 2025-07-18
- 浙江蘋果電腦測試設備 2025-07-18
- 工業物聯網G3-PLC芯片報價 2025-07-18
- 湖北機床柔性矩陣夾具 2025-07-18
- 常德企業租賃技術指導 2025-07-18
- 順德區綜合打印機租賃共同合作 2025-07-18
- 杭州巨型自動化控制系統 2025-07-18
- 福建KISSsoft軟件介紹 2025-07-18