山西中鹽核酸酶70950-150
大規模生產階段,AAV/LV載體生產流程跟抗體、疫苗類藥物的生產類似,主要包含上游培養、下游純化及制劑部分。上游培養分為質粒開發、細胞擴增、三質粒共轉染及病毒載體生產等步驟。下游純化分為細胞裂解釋放AAV病毒顆粒(可以通過去污劑、機械作用、高滲或凍融操作等)or收獲細胞上清液得到含LV病毒原液、加入核酸酶以減少宿主細胞核酸污染、澄清是通過離心或過濾等方法去除細胞碎片和雜質等、超濾濃縮以減少后續色譜純化體系、親合及離子交換等純化得到高純度病毒載體。制劑部分主要是超濾更換緩沖液、過濾除菌及制劑灌裝等。東臺中鹽核酸酶服務哪家好呢,歡迎咨詢上海倍篤生物 。山西中鹽核酸酶70950-150
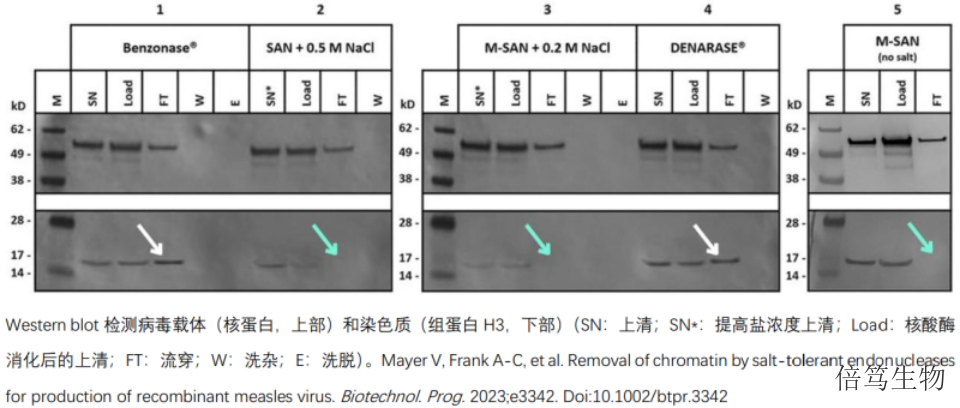
在傳統生物技術行業(如抗體、疫苗領域)使用的下游純化工藝步驟,已經用于慢病毒的大規模下游處理。主要是基于膜(過濾/澄清,利用切向流過濾TFF進行濃縮/滲濾,基于膜的色譜)和色譜(離子交換色譜IEC,親和色譜AC,體積排阻色譜SEC)的技術。這些不同的過程步驟的組合是可變的,在某些情況下,不同的純化方法可以用于相同的目的。此外,采用benzonase/M-SAN HQ中鹽核酸酶降解污染的DNA或者用于下游的一個步驟,或者用于病毒生產階段。陜西生理鹽條件中鹽核酸酶70950-202瓊脂糖膠結果顯示,M-SAN HQ中鹽核酸酶能將HCD消化成小于8nt的片段。

慢病毒大規模純化的捕獲步驟包括:膜過濾澄清,隨后切向流過濾/超濾或者體積排阻色譜濃縮。此外,需用核酸酶(benzonase或M-SAN HQ中鹽核酸酶)來去除細胞殘留的、質粒來源的DNA污染。這兩個步驟順序可以調整,依據項目工藝而定。兩種工藝路線各有優缺點:先用核酸酶消化的優點是可去除大的DNA片段,且后續步驟可以去除殘留核酸酶;但所用的核酸酶的量也非常大。與此相反,將核酸酶步驟后置的優點是大幅降低核酸酶的量(成本降低);但后面的步驟必須有將核酸酶去除的能力。此外,后期用核酸酶的缺點是核酸污染可能會結合慢病毒顆粒形成沉淀,進而導致慢病毒在純化中流失,從而影響得率。
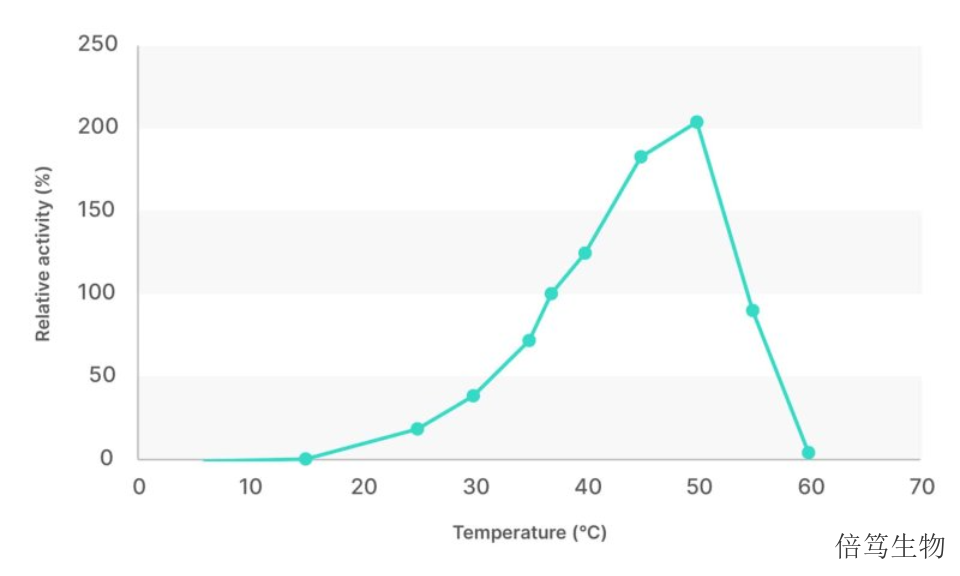
核酸酶活性受到很多因素影響,如鹽濃度、pH、底物、溫度等。因此,不同客戶、不同項目中核酸酶的使用條件都不一。目前,生物制藥行業對Benonase全能核酸酶的使用比較熟悉,如生理鹽或低鹽濃度、脫鹽操作等。對于大部分使用Benzonase的項目,使用M-SAN HQ中鹽核酸酶可以完全替代,而且溫度、Mg2+濃度等條件不用做任何調整,同樣酶量的M-SAN HQ對宿主細胞DNA(HCD)的去除效果更好、病毒載體得率更高。經過工藝優化后,可以將M-SAN HQ中鹽核酸酶的用量減少到原來的1/3-1/2,且HCD去除效果及產品得率更高。生理鹽濃度下,M-SAN HQ中鹽核酸酶性能優于常用核酸酶,對HCD的去除有些本質區別。
倫敦大學學院(UCL)的工藝開發團隊,在細胞藥物Car-T涉及的慢病毒(Lentivirus,LV)生產過程中,比較了Benzonase和M-SAN HQ中鹽核酸酶在酶活、酶切時間、各階段LV的穩定性等方面的表現,發現在生理鹽條件下M-SAN HQ中鹽核酸酶酶活更高、酶切時間更短,同時用納米顆粒分析(NTA)技術確認M-SAN HQ組得到的LV病毒顆粒聚集更少、穩定性更高。他們會繼續探究HCD是否影響LV的穩定性,及對LV侵染效率和生命周期是否有影響。通過更多研究,我們探究M-SAN HQ中鹽核酸酶助力LV生產的關鍵機制。安徽中鹽核酸酶哪家好呢,歡迎咨詢上海倍篤生物 。安徽等滲條件中鹽核酸酶
徐州中鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。山西中鹽核酸酶70950-150
基因藥物常用的AAV載體有三種生產方法,分別是三質粒瞬轉體系、桿狀病毒表達載體體系和包裝細胞體系。其中,20多年前開發的三質粒瞬轉表達技術仍然占據腺相關病毒AAV生產的主流地位,其三質粒分別是Helper質粒(含E2a/b、E4和VARNA基因)、目標基因表達質粒及輔助質粒(含Cap和Rep基因)。雖然AAV病毒載體的血清型不同,但AAV的生產流程基本一致,主要有質粒共轉宿主細胞HEK293、293細胞生產病毒顆粒、從細胞培養上清或/及細胞裂解液中收獲病毒載體、純化/制劑/無菌過濾/灌裝等流程。山西中鹽核酸酶70950-150
- 杭州70960-001中鹽核酸酶使用方法 2025-05-09
- 連云港倍篤生物中鹽核酸酶 2025-05-09
- 蚌埠70950-160中鹽核酸酶報價表 2025-05-09
- 衢州70950-150中鹽核酸酶工廠直銷 2025-05-09
- 蕪湖70921-150高鹽核酸酶廠家電話 2025-05-09
- 常州70950-202中鹽核酸酶工廠直銷 2025-05-09
- 溫州M-SAN HQ中鹽核酸酶供應商 2025-05-09
- 淮安70960-001中鹽核酸酶 2025-05-09
- 嘉興M-SAN HQ中鹽核酸酶采購 2025-05-09
- 嘉興SAN HQ高鹽核酸酶工廠直銷 2025-05-08
- 假眼需要多久 2025-05-09
- 黑龍江超輕超薄義眼片哪家好 2025-05-09
- 安徽氣氛真空爐哪里有賣的 2025-05-09
- 臨平區地磁空間水處理器生產廠家 2025-05-09
- 廈門VR仿真中醫針灸手法教學系統價格 2025-05-09
- 附近陪診服務價位 2025-05-09
- 福建眼摘假眼多少錢 2025-05-09
- 耐DMSO凍存管保質期 2025-05-09
- 浙江特殊氣氛真空爐碳管爐 2025-05-09
- 貴陽VR中醫針灸手法仿真測試系統生產廠家 2025-05-09